Introduktion af Gateway, et klinisk forsøg for Wilsons sygdom
Introduktion til GATEWAY, et klinisk forsøg for Wilsons sygdom
Wilsons sygdom er en sjælden genetisk sygdom, hvor overskydende kobber ophobes i kroppen og særligt i leveren og hjernen. Sygdommen skyldes mutationer i et gen, der kaldes ATP7B.
Hvis Wilsons sygdom ikke diagnosticeres tidligt og behandles korrekt, kan ophobningen af kobber forårsage alvorlige skader på organerne og resultere i svær funktionsnedsættelse med potentiel dødelig udgang. Dette betyder, at tidlig diagnosticering og hurtig behandling er meget vigtig.
Selvom der aktuelt findes medicinske behandlinger for Wilsons sygdom, skal forsøgsdeltagerne tage dem hele livet, og behandlingens virkning på nogle patienter ikke optimal. Derfor er der behov for nye behandlingsmuligheder.
VTX-801 er en ny behandling med genterapi for Wilsons sygdom, som i øjeblikket undersøges i GATEWAY. I det kliniske GATEWAY-forsøg undersøges sikkerheden, virkningen og varigheden af virkningerne for denne behandling.
Oplysninger om klinisk forsøg
Hvad er det kliniske GATEWAY-forsøg?
Navnet "GaTeWay" står for GenTerapi til Wilsons sygdom.
GATEWAY er et kliniske forsøg (også kaldet et "klinisk forskningsstudie") inden for genterapi, som udføres med patienter med Wilsons sygdom. Forsøget ønsker at vurdere, om forsøgsmedicinen VTX-801 er sikker, og finde den mest hensigtsmæssige dosis, som muligvis kan genetablere kroppens naturlige evne til at fjerne overskydende kobber.
Hvem udfører dette kliniske forsøg?
Det kliniske forsøg er sponsoreret af Vivet Therapeutics, en bioteknologisk virksomhed med base i Frankrig, som udvikler genterapier til sjældne leversygdomme.
Vivet samarbejder med Pfizer om
levering af VTX‐801, Vivets navnebeskyttede behandling mod Wilsons sygdom, til brug i dette kliniske fase 1/2‐ forsøg.
Hvad kan forsøgsdeltagerne forvente?
Forsøgsdeltagerne vil modtage en enkelt dosis af VTX-801, som bliver givet på hospitalet. Forsøgsdeltagerne skal derefter besøge forsøgscenteret på planlagte tidspunkter i løbet af det følgende år, så forsøgsteamet kan vurdere, hvordan de har det. Disse besøg er hyppigere i den tidlige fase af forsøget (første år) og bliver derefter mindre hyppige. Forsøget fortsætter i 4 år efter den første 1-års periode, hvilket er en altafgørende forudsætning for at forstå, hvor godt VTX-801 virker over tid.
Hvad er VTX-801-behandlingen?
VTX-801, som er den genterapi, der undersøges i forsøget, indeholder en korrigeret version af ATP7B-genet, som ikke fungerer korrekt hos patienter med Wilsons sygdom.
Den korrigerede version af genet pakkes ind i en vektor, som er en modificeret virus kaldet adeno-associeret virus (AAV), der er designet til at transportere genet ind i leverceller, uden at det forårsager infektion. Behandlingen gives som en enkelt infusion. VTX‐801 til forsøgsbrug fremstilles af Pfizer på en produktionsfacilitet i USA på vegne af Vivet Therapeutics.
Se videoen, og lær mere om, hvordan genterapi bekæmper årsagen til Wilsons sygdom (uddannelsesmateriale fra American Society of Gene & Cell Therapy)
Se, om du er egnet
Hvis du kan svare "ja" til de tre spørgsmål, kan du være egnet til at deltage i GATEWAY.
Hvis du er interesseret i at deltage, skal du kontakte den nærmeste deltagende klinik (se kort og kontaktoplysninger) for at få un dersøgt, om du opfylder de øvrige kriterier for deltagelse.
Hvor foregår GATEWAY-forsøget?
Forsøget foregår på flere klinikker i USA, Storbritannien, Tyskland og Danmark, som det er anført nedenfor. Kortet og klinikoplysningerne bliver opdateret, i takt med at den enkelte klinik bliver godkendt af de lokale myndigheder til at starte forsøget
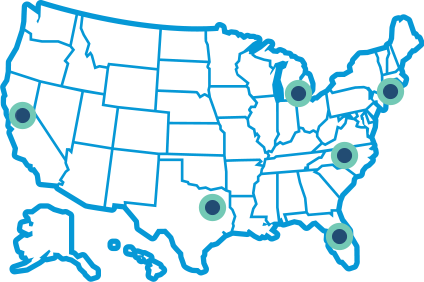
Kontakt en klinik i USA
University of California Davis
Dr. Valentina Medici
2000 Stockton Blvd
Sacramento, CA 95817
Sandeep Dhaliwal
(916) 734‐8696
University of Michigan Health System
Dr. Frederick Askari
1500 East Medical Center Dr. UH South F5161
Ann Arbor, MI 48109
Ashley Page
(734) 998-9966
Yale University School of Medicine
Dr. Michael Schilsky
310 Cedar Street
FMB 18
New Haven, CT 06520
Daksshi Hettiarachchi
(203) 737-5037
daksshi.hettiarachchi@yale.edu
Advent Health
Dr. Regino Gonzalez-Peralta
615 East Princeton Street
Orlando, Florida
Pamela Hedrick
(407) 303-9826
Pamela.Hedrick@AdventHealth.com
University of Texas Southwestern Medical Center
Dr. William Lee
5929 Harry Hines Boulevard
POB 1
Dallas, Texas
Amy Pugh
(214) 648-4412
Wake Forest School of Medicine
Dr. Sean Rudnick
Medical Center Boulevard Winston-Salem, NC 27157
Dee Faust
+1 336.713.1442
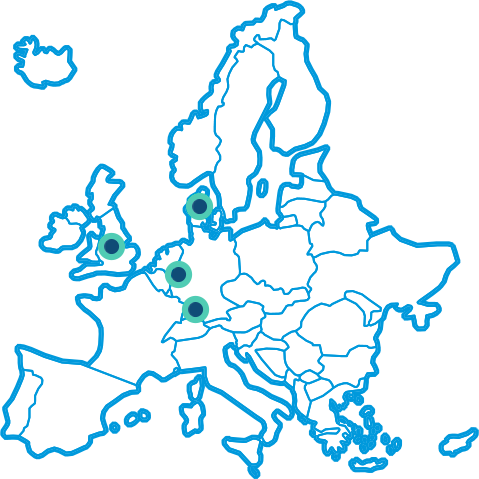
Kontakt en klinik i Europa
Aarhus Universitetshospital
Dr Thomas Damgaard Sandahl
Palle Juul-Jensens Boulevard 99
8200 Aarhus
Danmark
+45 5129 3791
Royal Surrey County Hospital
Pr. Aftab Ala
Egerton Road
Guilford,
Surrey GU2 7XX
United Kingdom
Pr. Aftab Ala
(+44) 1483 571 122
Universitätsklinikum Tübingen (UKT)
Pr. Ulrich Lauer
Otfried-Müller-Str. 10
72076 Tübingen
Deutschland
Prof. Ulrich Lauer
+49 7071-2983190
ulrich.lauer@med.uni-tuebingen.de
University Hospital Essen
Hufelandstrasse 55
45147 Essen
Deutschland
Prof. Hartmut Schmidt
+49 201 5990015
Ofte stillede spørgsmål
-
Vil det koste noget at deltage i forsøget?
Rejseudgifter og forsøgsrelaterede undersøgelser dækkes muligvis af sponsoren.
-
Vil alle, der deltager i det kliniske GATEWAY-forsøg, modtage genterapi?
Ja, der anvendes ingen placebogruppe i dette forsøg, så alle deltagere vil få den eksperimentelle
VTX-801-genterapi.
-
Hvad er genterapi?
Metoden for vores genterapi består i tilførsel af et korrigerende gen i levercellerne for at genetablere korrekt leverfunktion og fjerne overskydende kobber.
For at et gen kan trænge ind i en celle, skal det pakkes ind i et transportmiddel, som kaldes en "vektor".
Virusser fungerer godt som vektorer, da de har nemt ved at komme ind i vores celler. Forskere kan udvikle egnede versioner af virusser til brug som vektorer til dette formål. De er harmløse og vil ikke forårsage sygdom, når de bruges i mennesker. For at kunne gøre dette skal forskerne erstatte det DNA, som naturligt findes i virusset, med det gen, som skal bruges til at behandle sygdommen.
Du kan lære mere om genterapi for Wilsons sygdom i uddannelsesmaterialet fra American Society of Gene & Cell Therapy
-
Hvad kræver det at deltage i det kliniske GATEWAY-forsøg?
Størstedelen af besøgene er planlagt til at finde sted i løbet af det første år, og forsøgets fulde varighed er 5 år. I løbet af det første år er nogle af besøgene, hvor der indsamles blod- og urinprøver, planlagt til at finde sted hjemme hos dig selv for at gøre det nemmere for dig.
-
Hvor mange patienter kan der deltage i det kliniske forsøg?
Vi søger cirka 16 patienter, som ønsker at deltage i GATEWAY.
-
Hvem beslutter, hvem der kan deltage i det kliniske forsøg?
GATEWAY-forsøgsprotokollen, der er udarbejdet af sponsoren og godkendt af eksperter i Wilsons sygdom og de kompetente myndigheder (herunder de amerikanske sundhedsmyndigheder FDA), definerer kriterierne for deltagelse. Ud fra disse kriterier beslutter komitéen for forsøgsdeltagelse, som består af forskere (investigatorer) og andet fagligt relevant personale, hvem der kan deltage i forsøget.
-
Hvorfor er det kun voksne patienter med stabil Wilsons sygdom, der kan deltage i GATEWAY?
I det første kliniske forsøg er det kun voksne med stabil Wilsons sygdom, der kan deltage, men når der er indsamlet tilstrækkelige data fra GATEWAY-forsøget, vil der muligvis blive arrangeret andre forsøg for andre patientpopulationer.
-
Kan genterapiproduktet VTX-801 fås på andre måder end ved at deltage i GATEWAY?
Da VTX-801 er en forsøgsbehandling, er den i øjeblikket udelukkende tilgængelig for patienter, der deltager i GATEWAY.
VTX-801 vil kun være tilgængelig i forbindelse med kliniske forsøg, indtil behandlingen er færdigudviklet, og de kompetente myndigheder har afgjort, om den kan godkendes til kommerciel anvendelse. Hele processen tager typisk et par år fra starten af det første kliniske forsøg.
-
Hvor fremstilles VTX‐801?
VTX‐801 til forsøgsbrug fremstilles af Pfizer på en produktionsfacilitet i USA på vegne af Vivet Therapeutics.
Kontakt: info@vivet-therapeutics.com
GATEWAYs Politik for beskyttelse af persondata | Brugsvilkår
Webstedet er designet af Boston Web Partners










