Einführung von Gateway, einer klinischen Studie für die Wilson-Krankheit
GATEWAY: eine klinische Studie für die Wilson-Krankheit
Die Wilson-Krankheit ist eine seltene genetische Störung, bei der sich überschüssiges Kupfer im Körper, insbesondere in der Leber und im Gehirn, ansammelt. Die Krankheit wird durch Mutationen in einem Gen namens ATP7B verursacht.
Wenn die Wilson-Krankheit nicht frühzeitig diagnostiziert und angemessen behandelt wird, kann die Ansammlung von Kupfer schwere Schäden an den Organen verursachen und zu schweren Behinderungen und möglicherweise zum Tod führen. Das bedeutet, dass eine frühzeitige Diagnose und eine schnelle Behandlung sehr wichtig sind.
Zwar gibt es derzeit medikamentöse Behandlungen für die Wilson-Krankheit, doch müssen die Patienten diese lebenslang einnehmen, und bei einigen Patienten ist das therapeutische Ansprechen nicht optimal. Aus diesen Gründen sind neue therapeutische Optionen wünschenswert.
VTX-801 ist eine neue Gentherapie zur Behandlung der Wilson-Krankheit, die derzeit in GATEWAY untersucht wird. In der klinischen Studie GATEWAY wird untersucht, wie sicher, wirksam und nachhaltig die Wirkung dieser Behandlung ist.
Informationen zur klinischen Studie
Was ist die klinische Studie GATEWAY?
Der Name ‘GaTeWay’ steht für Gene Therapy for Wilson Disease (auf Deutsch: Gentherapie für die Wilson-Krankheit).
GATEWAY ist eine klinische Gentherapiestudie (auch als „klinische Forschungsstudie“ bezeichnet), die bei Patienten mit Morbus Wilson durchgeführt wird. Es soll damit ermittelt werden, ob das Studienmedikament VTX-801 sicher ist und welche Dosis am besten geeignet ist, um die Ausscheidung von überschüssigem Kupfer auf natürlichem Wege dauerhaft wiederherzustellen.
Wer führt diese klinische Studie durch?
Die klinische Studie wird von Vivet Therapeutics gesponsert, einem Biotechnologieunternehmen mit Sitz in Frankreich, das Gentherapien für seltene Lebererkrankungen entwickelt. Vivet arbeitet mit Pfizer bei der klinischen Bereitstellung von VTX-801, der von Vivet entwickelten Behandlung für die Wilson-Krankheit, für diese klinische Phase 1/2-Studie zusammen.
Was sollten Studienteilnehmer erwarten?
Die Patienten erhalten eine Einzeldosis von VTX-801, die im Krankenhauls verabreicht wird. Die Patienten werden dann im Laufe des darauf folgenden Jahres zu geplanten Terminen in ihr Studienzentrum kommen, damit das Studienteam beurteilen kann, wie es ihnen geht. Diese Besuche werden in der Anfangsphase der Studie (erstes Jahr) häufiger stattfinden. In der folgenden Zeit wird die Anzahl der Besuche wird abnehmen. Die Studie wird nach dem anfänglichen 1-Jahres-Versuchszeitraum 4 Jahre lang fortgesetzt. Dies ist entscheidend, um herauszufinden, wie gut VTX-801 im Laufe der Zeit wirkt.
Was ist die Behandlung VTX-801?
VTX-801, die in dieser Studie untersuchte Gentherapie, enthält eine korrigierende Version des ATP7B-Gens, das bei Patienten mit der Wilson-Krankheit eine Fehlfunktion aufweist.
Die korrigierende Version des Gens ist in einem Vektor verpackt. Dabei handelt es sich um ein modifiziertes Virus namens Adeno-assoziiertes Virus (AAV), das so entwickelt wurde, dass es das Gen in Leberzellen einschleust, ohne eine Infektion zu verursachen. Die Behandlung wird als einmalige intravenöse Infusion verabreicht. VTX-801 für die klinische Versorgung wird von Pfizer in einer US-amerikanischen Produktionsstätte im Auftrag von Vivet Therapeutics hergestellt.
Sehen Sie sich das Video an, um mehr darüber zu erfahren, wie mithilfe von Gentherapie die Ursache der Wilson-Krankheit bekämpft werden soll (Aufklärungsmaterial der American Society of Gene and Cell Therapy).
Teilnahmeberechtigung prüfen
Wenn Sie drei Fragen mit „Ja“ beantwortet haben, kommen Sie möglicherweise für eine Teilnahme an GATEWAY in Frage.
Wenn Sie an einer Teilnahme interessiert sind, wenden Sie sich bitte an das nächstgelegene teilnehmende klinische Prüfzentrum (siehe Karten und Kontaktdaten), um die weiteren Teilnahmekriterien zu prüfen.
Wo findet die GATEWAY-Studie statt?
Die Studie wird an mehreren klinischen Prüfzentren in den Vereinigten Staaten, Großbritannien, Deutschland und Dänemark durchgeführt, wie unten angegeben. Die Karte und die Details der Prüfzentren werden aktualisiert, sobald die örtlichen Behörden die Genehmigung für den Beginn der Studie an einem neuen Prüfzentrum erteilt haben.
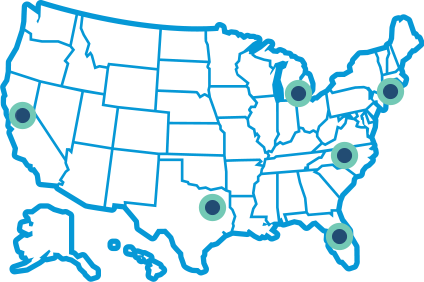
Ansprechpartner für Prüfzentren in den USA
University of California Davis
Dr. Valentina Medici
2000 Stockton Blvd
Sacramento, CA 95817
Sandeep Dhaliwal
(916) 734‐8696
University of Michigan Health System
Dr. Frederick Askari
1500 East Medical Center Dr. UH South F5161
Ann Arbor, MI 48109
Ashley Page
(734) 998-9966
Yale University School of Medicine
Dr. Michael Schilsky
310 Cedar Street
FMB 18
New Haven, CT 06520
Daksshi Hettiarachchi
(203) 737-5037
daksshi.hettiarachchi@yale.edu
Advent Health
Dr. Regino Gonzalez-Peralta
615 East Princeton Street
Orlando, Florida
Pamela Hedrick
(407) 303-9826
Pamela.Hedrick@AdventHealth.com
University of Texas Southwestern Medical Center
Dr. William Lee
5929 Harry Hines Boulevard
POB 1
Dallas, Texas
Amy Pugh
(214) 648-4412
Wake Forest School of Medicine
Dr. Sean Rudnick
Medical Center Boulevard Winston-Salem, NC 27157
Dee Faust
+1 336.713.1442
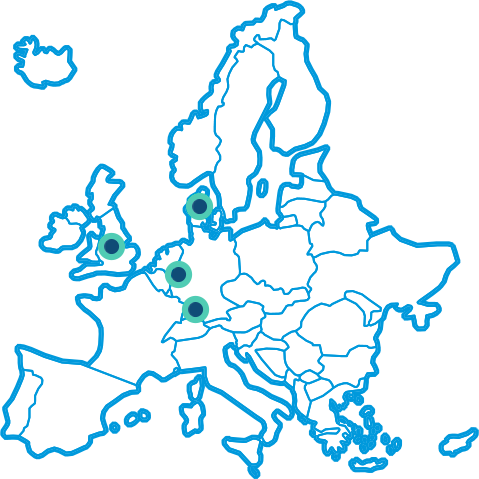
Wenden Sie sich an eine europäische klinischen Prüfzentren
Aarhus Universitetshospital
Dr Thomas Damgaard Sandahl
Palle Juul-Jensens Boulevard 99
8200 Aarhus
Danmark
+45 5129 3791
Royal Surrey County Hospital
Pr. Aftab Ala
Egerton Road
Guilford,
Surrey GU2 7XX
United Kingdom
Pr. Aftab Ala
(+44) 1483 571 122
Universitätsklinikum Tübingen (UKT)
Pr. Ulrich Lauer
Otfried-Müller-Str. 10
72076 Tübingen
Deutschland
Prof. Ulrich Lauer
+49 7071-2983190
ulrich.lauer@med.uni-tuebingen.de
University Hospital Essen
Hufelandstrasse 55
45147 Essen
Deutschland
Prof. Hartmut Schmidt
+49 201 5990015
Häufig gestellte Fragen
-
• Wird die Teilnahme an der Studie etwas kosten?
Reisekosten und studienbezogene Tests werden möglicherweise vom Sponsor übernommen.
-
• Wird jeder, der an der klinischen GATEWAY-Studie teilnimmt, eine Gentherapie erhalten?
Ja, in dieser Studie gibt es keinen Placebo-Arm, so dass alle Teilnehmer die experimentelle Gentherapie VTX-801 erhalten werden.
-
Was ist Gentherapie?
Unser gentherapeutischer Ansatz beinhaltet die Einschleusung eines korrigierenden Gens in die Leberzellen, um die ordnungsgemäße Leberfunktion wiederherzustellen und überschüssiges Kupfer zu entfernen.
Damit ein Gen in eine Zelle gelangen kann, muss es in ein Transportvehikel verpackt werden, das auch als „Vektor“ bezeichnet wird.
Viren eignen sich gut als Vektoren, weil sie leicht in unsere Zellen eindringen können. Wissenschaftler können zu diesem Zweck geeignete Versionen von Viren als Vektoren entwickeln. Diese sind harmlos und verursachen keine Krankheiten, wenn sie bei Menschen angewendet werden. Dazu ersetzen die Wissenschaftler die DNA, die natürlicherweise im Virus vorhanden ist, durch das Gen, das zur Behandlung der Krankheit verwendet werden soll.
Um mehr über die Gentherapie der Wilson-Krankheit zu erfahren, lesen Sie das Aufklärungsmaterial der American Society of Gene & Cell Therapy.
-
• Was beinhaltet die Teilnahme an der klinischen GATEWAY-Studie?
Die Gesamtdauer der Studie beträgt 5 Jahre und die meisten der Studienbesuche sind für das erste Jahr geplant. Im ersten Jahr finden einige der Besuche, bei denen Blut- und Urinproben genommen werden, nicht im Krankenhaus, sondern bei Ihnen zu Hause statt. Wir möchten Ihnen damit die Teilnahme leichter machen.
-
• Wie viele Patienten können an der klinischen Studie teilnehmen?
Wir benötigen ungefähr 16 Patienten, die an GATEWAY teilnehmen möchten.
-
• Wer entscheidet, wer an der klinischen Studie teilnehmen darf?
Die Aufnahmekriterien sind im GATEWAY-Studienprotokoll angegeben, das vom Sponsor erstellt und mit Experten für die Wilson-Krankheit und den zuständigen Aufsichtsbehörden (einschließlich der FDA) abgestimmt wurde. Auf der Grundlage dieser Kriterien entscheidet das Komitee zur Aufnahme in die Studie, das sich aus Prüfern und Co-Prüfern zusammensetzt, wer an der Studie teilnehmen darf.
-
• Warum können nur erwachsene Patienten mit stabiler Wilson-Krankheit in GATEWAY aufgenommen werden?
An dieser ersten klinischen Studie können nur Erwachsene mit stabiler Wilson-Krankheit teilnehmen. Sobald jedoch genügend Daten in GATEWAY erfasst wurden, können weitere Studien organisiert werden, um andere Patientengruppen zu untersuchen.
-
• Ist das Gentherapieprodukt VTX-801 auch außerhalb von GATEWAY erhältlich?
Da es sich bei VTX-801 um ein Prüfpräparat handelt, ist es derzeit ausschließlich für Patienten verfügbar, die in GATEWAY aufgenommen werden.
VTX-801 wird außerhalb der klinischen Studien nicht erhältlich sein, bis die Entwicklung abgeschlossen ist und die zuständigen Behörden entschieden haben, ob es für die Vermarktung zugelassen werden kann. Der gesamte Prozess dauert in der Regel einige Jahre nach Beginn der ersten klinischen Studie.
-
Wo wird VTX-801 hergestellt?
VTX-801 für die klinische Versorgung wird von Pfizer in einer US-amerikanischen Produktionsstätte im Auftrag von Vivet Therapeutics hergestellt.
Kontakt: info@vivet-therapeutics.com
GATEWAY-Datenschutzrichtlinie | Nutzungsbedingungen
Website-Design von Boston Web Partners









